-
 CoⅢ 정팔면체 배위 화합물 CoNH35Xn+ X NH3
CoⅢ 정팔면체 배위 화합물 CoNH35Xn+ X NH3 -
무기화학실험
Co(Ⅲ) 정팔면체 배위 화합물: [Co(NH3)5X]n+ [X: NH3 (n=3), Cl(n=2), CO3 (n=1)]와 [Co(en)3I3+]의 착염 합성
7. Results
실험 1. Hexaammine cobalt (Ⅲ) chloride
결과처리 및 결과 분석
① 수득률 구하기
(1) 실험에서 사용된 시료의 몰 수
반응식 : 4CoCl2 + 4NH4Cl + 20NH3 +O2 → 4[Co(NH3)6]Cl3 + 2H2O
CoCl2 mole 수 = 쓰인 CoCl2 · 6H2O의 질량 / CoCl2 · 6H2O의 분자량
= {6g} over {eqalign{237.93g/mol#
}} = 0.025mol
9. 참고문헌
네이버 지식백과
이공학을 위한 무기화학 실험
- 실험 다량 실험값 무게 분자량 수득률, CoⅢ 정팔면체 배위 화합물 CoNH35Xn+ X NH3
-
 Fluorescence Spectrum and Rate of Electr
Fluorescence Spectrum and Rate of Electr-
Fluorescence Spectrum and Rate of Electron Transfer Reaction by Quenching 결과보고서
결과
1) Fluorescence emission spectrum, Fluorescence excitation spectrum, UV Absorption spectrum 세 종류의 peak그래프를 찍는다.
2) 세 종류의 그래프를 비교하고 분석한다.
3) [Fe3+],[Cu2+] 농도에 대한 emission Intensity ratio(I0/I) 를 plot하여 속도상수의 비(kq/ks )를 구한다.
▶ 실험A. fluorescein의 UV Absorption spectrum 측정
최대 peak: 490nm / 흡광도 : 2.51820
▶ 실험B. fluorescence emission spectrum 측정
excita...
- 최대 용액 실험 측정 설정 결과, Fluorescence Spectrum and Rate
-
 Liquid-Vapor Equilbrium Azeotropic Mixtu
Liquid-Vapor Equilbrium Azeotropic Mixtu-
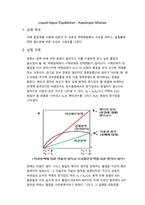
Liquid-Vapor Equilibrium : Azeotropic Mixture
실험 목표
아베 굴절계를 사용해 성분이 두 성분의 액체혼합물의 조성을 정하고, 굴절률에 대한 끓는점에 따른 조성의 그래프를 그린다.
실험 이론
- 굴절률 실험 액체 물질 성분 법칙, Liquid-Vapor Equilbrium Azeotr
-
 Effect of Ionic Strength on Solubility_결
Effect of Ionic Strength on Solubility_결-
Effect of Ionic Strength on Solubility
결과
1.1 KSCN 첨가량(mol)
NO3농도(M) Na
0.1M KSCN첨가량(mL)
KSCN 몰수(mol)
0
6.0
0.00060
0.05
7.2
- 첨가량 이론값 결과 계수 모두 평균, Effect of Ionic Strength on So
-
 Determination of Equilibrium_Adsorption
Determination of Equilibrium_Adsorption -
Equilibrium, Activated Carbon
실험 목표
활성탄소를 사용해 아세트산이 흡착되는 것을 확인할 수 있으며 평형상수 K를 구할 수 있고 흡착의 원리를 이해할 수 있다. 또한 Langmuir 등온 흡착식이 성립하는 지를 판단할 수 있다.
실험 이론
- 흡착 물질 실험 액체 표면 등온, Determination of EquilibriumAd
-
 Liquid-Vapor Equilibrium Azeotropic Mixt
Liquid-Vapor Equilibrium Azeotropic Mixt-
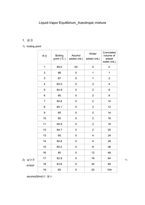
Liquid-Vapor Equilibrium_Azeotropic mixture
결과
boiling point
측정
Boiling point (°C )
Alcohol added (mL)
Water added (mL)
Cumulated volume of added water (mL)
1
89.5
50
0
0
2
88
0
1
- 증류수 용액 몰분율 비율 실험 증기, Liquid-Vapor Equilibrium Azeot
-
 The visible spectra of Cyanine Dyes_예비보고
The visible spectra of Cyanine Dyes_예비보고-
The Visible Spectra of Cyanine Dyes
실험 목표
시아닌염료의 가시광선 영역에 해당하는 흡수 스펙트럼을 획득한 후, 이 흡수 스펙트럼에서 발견된 흡수대의 위치를 electron-in-a-box model을 사용하여 추측한다. Method 안의 염료의 투광도를 통해 흡광도를 구할 수 있으며 이를 통해, 서로 다른 농도를 가지는 용액의 흡광도를 계산한다. 스펙트럼을 UV Spectrophotometer로 찍은 다음 최대 흡수파장을 얻고 이론값과 실험값의 상대오차를 계산한다.
실험 이론
- 흡수 이때 흡광도 염료 실험 에너지, The visible spectra of Cyanine
-
 Equilibrium activated carbon_결과보고서
Equilibrium activated carbon_결과보고서-
Equilibrium, activated carbon
1.결과
1-1.NaOH용액의 표준화
표1.NaOH의 표준화
사용된 NaOH의 부피(mL)
22mL
적정에 사용된 KHP의 부피(mL)
25mL
NaOH의 표준 노르말 농도(N)
0.0890
-사용된 KHP:0.400g(분자량: 204.23g/mol)
사용된 NaOH부피:22mL
0.1N=0.1eq/1000mL이므로
(0.1eq/1000mL)*XKHPmL=0.400g/(204.23g/mol)
XKHP=19.586mL
-NV=N’V’이용
0.1N*19.586mL=XNaOHN*22mL
XNaOH=0.0890N
- 부피 몰수 표준화 표준 흡착 사용, Equilibrium activated carbon결과보
-
 The visible Spectra of Cyanine Dyes_결과보고
The visible Spectra of Cyanine Dyes_결과보고-
The visible spectra of Cyanine Dyes
결과
식 (1)
이때, m은 전자의 질량이며 그 값은 9.109kg이다.
c는 빛의 속도이며 그 값은 2.998m/s이다.
l은 탄소와 탄소 사이의 1.5중 결합 길이이며 그 값은 1.39m이다.
h는 플랑크 상수이며 그 값은 6.626Js이다.
J는 conjugation을 하는 이중 결합의 개수이다.
이론값
1,1’-Diethyl-2,2’-cyanine iodide (J=1, 1ml를 250ml 메탄올에 녹인 것 & 1ml를 100ml 메탄올에 녹인 것)
- 계수 몰흡광 흡광도 그 용액 메탄올, The visible Spectra of Cyanine
-
 Analysis of IR Spectrum of HClg_예비보고서
Analysis of IR Spectrum of HClg_예비보고서-
Analysis of IR Spectrum of HCI(g)
1.실험 목적
이 실험은 고체시료의 IR Spectrum을 측정해 작용기를 파악하고, 기체 HCl분자 의 IR spectrum을 관찰하여 결합길이와 힘상수를 얻는다. 그리고 이 과정을 통해 anharmonicity constant와 vibration-rotation interaction, centrifugal distortion constant를 구해본다.
2.실험 이론
그림1. 빛의 스펙트럼
적외선 영역의 파수는 대략적으로 2900 cm-1~10 cm-1이며 파장으로 치면 770 nm~1000 μm를 포함한다. 적외선 영역의 빛은 자외선과 가시광선보다 에너지가 낮기 때문에 들뜨지 않고 분자가 진동하거나 회전을 하게 된다.
그림2. 분자의 신축진동과 굽힘진동의 예시
분자가 진동을 할 때 신축진동을 하게 되면 원자와 원자 사이의 결합 길이가 달라지고 굽힘 진동을...
- 진동 에너지 분자 준위 진동자 이때, Analysis of IR Spectrum of HCl
이메일 무단수집 거부
 본 웹사이트에 게시된 이메일 주소가 전자우편 수집 프로그램이나 그 밖의 기술적 장치를 이용하여 무단으로 수집되는 것을 거부하며, 이를 위반시 정보통신망법에 의해 형사처벌됨을 유념하시기 바랍니다. [게시일 2003년 4월 2일]
본 웹사이트에 게시된 이메일 주소가 전자우편 수집 프로그램이나 그 밖의 기술적 장치를 이용하여 무단으로 수집되는 것을 거부하며, 이를 위반시 정보통신망법에 의해 형사처벌됨을 유념하시기 바랍니다. [게시일 2003년 4월 2일]
 CoⅢ 정팔면체 배위 화합물 CoNH35Xn+ X NH3
CoⅢ 정팔면체 배위 화합물 CoNH35Xn+ X NH3  Fluorescence Spectrum and Rate of Electr
Fluorescence Spectrum and Rate of Electr Liquid-Vapor Equilbrium Azeotropic Mixtu
Liquid-Vapor Equilbrium Azeotropic Mixtu Effect of Ionic Strength on Solubility_결
Effect of Ionic Strength on Solubility_결 Determination of Equilibrium_Adsorption
Determination of Equilibrium_Adsorption  Liquid-Vapor Equilibrium Azeotropic Mixt
Liquid-Vapor Equilibrium Azeotropic Mixt The visible spectra of Cyanine Dyes_예비보고
The visible spectra of Cyanine Dyes_예비보고 Equilibrium activated carbon_결과보고서
Equilibrium activated carbon_결과보고서 The visible Spectra of Cyanine Dyes_결과보고
The visible Spectra of Cyanine Dyes_결과보고 Analysis of IR Spectrum of HClg_예비보고서
Analysis of IR Spectrum of HClg_예비보고서 충북대_일반물리학및실험1_6주차_운동량과충격량
충북대_일반물리학및실험1_6주차_운동량과충격량  [조림학] 수간석해를 통한 간벌효과 분석
[조림학] 수간석해를 통한 간벌효과 분석  [분석화학실험] EDTA Titration (우유속의 칼슘정량) 결과레포트
[분석화학실험] EDTA Titration (우유속의 칼슘정량) 결과레포트  충북대_일반물리학및실험1_7주차_역학적에너지보존
충북대_일반물리학및실험1_7주차_역학적에너지보존  화학실험보고서 - 이산화탄소의 분자량
화학실험보고서 - 이산화탄소의 분자량  [일반화학실험보고서] 일반화학실험보고서-이산화탄소분자량
[일반화학실험보고서] 일반화학실험보고서-이산화탄소분자량  토목지질학 - 암석의 분류에 대해서
토목지질학 - 암석의 분류에 대해서  [일반물리학실험1] 운동량 보존 법칙
[일반물리학실험1] 운동량 보존 법칙  진동공학/중간고사/족보(2016)/금오공대(금오공과대학교)/기계공학과
진동공학/중간고사/족보(2016)/금오공대(금오공과대학교)/기계공학과  알코올의 증류(일반화학 실험보고서)
알코올의 증류(일반화학 실험보고서)  [A+] 소리간섭실험보고서
[A+] 소리간섭실험보고서  경문사 - 생명과학을 위한 수학1 솔루션2 - 2장 연습문제
경문사 - 생명과학을 위한 수학1 솔루션2 - 2장 연습문제  [수학] 음함수와 음함수 방정식
[수학] 음함수와 음함수 방정식  [현대과학] 자연과학 분야에서의 아리스토텔레스
[현대과학] 자연과학 분야에서의 아리스토텔레스  [생물실험] 양파 뿌리의 체세포분열과 호밀 수분의 감수분열
[생물실험] 양파 뿌리의 체세포분열과 호밀 수분의 감수분열  일반물리학 정리 및 요약
일반물리학 정리 및 요약  단체급식 -시장조사와 발주서 작성
단체급식 -시장조사와 발주서 작성  일반물리학실험(1) 선운동량 보존법칙 결과보고서
일반물리학실험(1) 선운동량 보존법칙 결과보고서  논문양식, 처음 논문쓸때 참고될 문서
논문양식, 처음 논문쓸때 참고될 문서  기계요소설계I(사람의 손으로 돌리는 자동차용 재키를 설계하시오)
기계요소설계I(사람의 손으로 돌리는 자동차용 재키를 설계하시오)