Yamada를 새로운 위치에 선정했을 때, GSK의 CEO, Jean-Pierre Garnier는 제약 연구 개발 GSK 의 감소하는 생산성이 직면하고 있는 가장 큰 문제인 의약 R&D 부서의 생산성 감소에 대한 해결을 위해 창조적인 메커니즘에 대해서 생각하라고 장려하였다. 당시 SmithKline Beecham의 CEO였던 Garnier는 과거에 Yamada와 가깝게 일했었고, Yamada가 GSK 위해서만 아니라 전체 제약 업계 전반에 걸쳐서 생산성 규모 문제에 대해 예민한 감각을 가졌다고 확신했다. Yamada의 관점에서 전통적으로 산업을 주도해왔던 대형회사들은 과도한 관료제, 기능적 구조 내부와 구조를 가로지는 의사소통의 미비함, 그가 “기업가 정신”이라 칭한 일반적인 부재 때문에 곤경에 처해있었다.
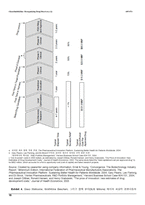
GSK 합병 발표 이후 3 주 동안, Yamada는 이미 GSK의 약물 개발에 대한 극적인 재조정을 구상해두었다. 그의 제안은 GSK의 약 1,900명의 약품 개발자들을 각각 하나에서 세가지의 치료 영역에 초점을 맞춘 여섯개의 "약물 개발특화센터(CEDDS)"로 나누는 것이다. Glaxo wellcome과 Smithkline beecham이 현재 이용할 수 있는 연구 과학자에 필수적으로 의존하는 반면, Yamada는 GSK의 CEDDs가 특정 분야에서 규모의 이점을 활용하여 연구 생산성을 크게 향상시키고 다른 것에 초점을 맞추는 것을 보장할 수 있다고 느꼈다. 그는 이미 각 수석 R & D에 임원으로 구성된 전통조직인 Garnier 와 R & D 통합위원회에서 자신의 구조 조정 계획의 광범위한 개요에 대한 사전 지원을 받고 있었다. 현재, 그는 합병 계획의 종결을 위해 새로운 구조의 세부 정보를 시간 내에 구현할 필요가 있었다. 그는 겨우 다섯 달의 시간이 남아 있었다.
Robert S. Huckman 교수와 Eli. P. Strick 연구 협회에서 함께 이번 사례를 준비했다. HBS 사례들은 오로지 수업 토의용으로만 제작되었다. 사례들은 특정 기업에 대한 지지, 기초 자료의 원천, 혹은 효율적 또는 비효율적 경영에 대한 표현을 의도로 제작되지 않았다
제약 산업
2000년에, 제약 업계는 조정 상태였었다. 미국 노인 인구의 증가와 수명의 연장은 건강 관리 제품과 서비스 의 개선에 대한 요구를 증대시켰고, 그 중 특히 처방 의약품에 대한 수요가 강화할 될 것으로 예상했었다. 2000년 글로벌 제약 판매는 1999년1에 비해 최대 8%오른 3600억 달러에 도달할 것으로 예상했다. 스탠다드 & 푸어스의 계획안에 따르면, 미국의 의약품 지출은 2002년에서 2006년 사이에 거의 11%의 연간 비율로 성장할 것으로 예상했었다. 그러나 시장의 성장에도 불구하고, 많은 최고 판매 의약품들이 특허 삶의 끝에 도달하게 되었고, 상황은 일반적인 경쟁2에 직면하게 된다. 2001년에서 2005년 사이에 약 3백50억 달러의 총 연간 매출액을 기록한 브랜드 의약품은 특허 보호3를 잃을 것으로 예상했었다. 특허 문제 외에도, 제약 회사는 점점 더 커지고 있는 수요로 인해 정부, 관심 보험사 및 의료 소비자들로부터 처방전 의약품 비용을 낮추라는 가격 압력에 직면했었다.
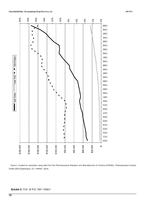
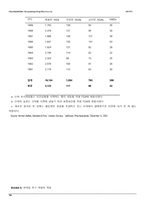
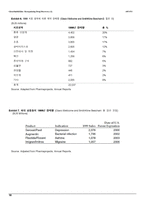
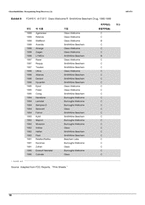
그들의 시장 점유율을 보호하기 위해, 제약 회사들은 좀더 많은 새로운 약 개발의 희망에 R & D 투자에 그들의 투자를 지속적으로 늘렸다. 그러나 많은 산업 회의론자들은 지출의 증가는 생산의 극적인 증가라고 여전히 해석 된다고 빠르게 지적하였다. 2000 및 2001에 대한 생산 예상을 보면 이러러한 많은 회의론자들은 희미하게 비치는 산업의 "생산성 위기"에 대해 걱정하였다. 1989년도와 1999년도 사이에, 미국 제약 연구 회사는 대략 1,850억달러를 R & D 에 투자하였고, 1999년도에만 1,550달러 판매량과 비교하여 2백 40억달러 이상을 지출하였다. 4 Exhibit 1 은 1970 년부터 산업의 매출 및 R & D 지출의 역사적 성장을 보여준다. Exhibit3은 1990 년대 미국 식품 의약청 (FDA)에의한 약물 승인 활동에 관한 데이터를 제공한다. 이 기간 동안, FDA는 288개의 새로운 분자 독립체(NMEs)를 포함하는 약 800개의 신약 응용 프로그램을 (NDAs)승인하였다.(Exhibit 2)567
약물의 발견과 개발 과정
1,Herman Saftlas, “Healthcare: Pharmaceuticals,” Standard & Poor’s Industry Surveys, December 16, 1999.
2 Weeks after Eli Lilly’s patent for its leading antidepressant, Prozac, expired in August 2001, generic versions took over 80% of the drug’s prescriptions.
3 Herman Saftlas, “Healthcare: Pharmaceuticals,” Standard & Poor’s Industry Surveys, December 21, 2000.

- 오늘 본 자료가 없습니다.
- [기업윤리] 포드핀토사례
- 싸이언 광고 분석
- [A+레포트] 경영정보시스템_포터의 경쟁세력모형 이론에 대해 설명하고, 관심 산업분야에서 새로운 정보기술에 의한 산업변화를 경쟁세력모형을 이용하여 설명하시오_포터경쟁세력모형
- 현재 산업현장에서는 4차 산업혁명 시대라는 패러다임에 발맞추어 기업의 생산성 향상 및 효율성을 높이기 위해 다양한 방법을 활용해보고 있는데, 생산관리 1~4주차의 내용을 바탕으로 하여 새로운 전략수립과 새로운 제품의 설계, 공정설계, 생산능력 향상, 중 하나의 주제를 선택하여 기업의 생산성 향상 및 효율성을 높이기 위한 주제로 의견을 기술해보시오.
- 국제개발협력의 실패사례와 대안
해당 정보 및 게시물의 저작권과 기타 법적 책임은 자료 등록자에게 있습니다. 위 정보 및 게시물 내용의 불법적 이용,무단 전재·배포는 금지되어 있습니다. 저작권침해, 명예훼손 등 분쟁요소 발견 시 고객센터에 신고해 주시기 바랍니다.

















 분야
분야

