분자간 힘
물질의 상태
물질 상태 사이의 근본적인 차이: 분자간 인력의 세기.
분자간 힘이 클수록, 분자간 거리는 더욱 가까워진다.
고체나 액체를 응축상 (condensed phases) 이라고 한다.
물질 상태의 차이
어떤 상태의 물질?
이 질문의 답이 크게 의존하는 두 가지:
입자의 운동 에너지 사이의 균형
입자간 인력
분자간 힘
분자간 인력은 화합물을 결속시켜주는 분자내 인력만큼 세지는 않다.
분자간 인력을 반영하는 물리적 성질들:
끓는점, 녹는점, 증기 압력, 압력, 점도.
분자간 힘의 종류
아래로 갈수록 센 힘:
분산력 dispersion forces (또는 London 분산력)
쌍극자-쌍극자 힘 dipole-dipole forces
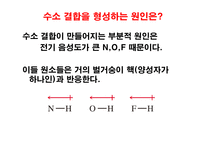
수소 결합 hydrogen bonding (특별한 쌍극자-쌍극자 힘)
이온-쌍극자 힘 ion-dipole forces
[주] 처음 두 종류의 총괄명칭: van der Waals 힘
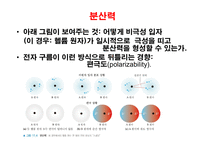
분산력
아래 그림이 보여주는 것: 어떻게 비극성 입자
(이 경우: 헬륨 원자)가 일시적으로 극성을 띠고 분산력을 형성할 수 있는가.
전자 구름이 이런 방식으로 뒤틀리는 경향: 편극도(polarizability).

- 오늘 본 자료가 없습니다.
- 주제 소비자 구매의사결정과정의 개념과 소비자 구매의사결정과정을 문제인식에서부터 구매 후까지의 행동을 사례를 통해 제시해 보시오
- [국제관계론]OECD의 현황과 문제점 그리고 해결방안
- 영화 기생충을 보고 사회복지사로서 개입 방법 1 부자 집 개입 방법과 2 반지하 집 사는 사람들의 개입 방법에 대해 기술하시오
- 가족상담및가족치료-나의 원가족을 가계도로 도식화해보고 보웬의 다세대가족치료모델의 자아분화의 개념을 적용하여 자기를 깊이있게 성찰해보세요
- 3주 1차시에 아동관찰 방법 중 서술식 관찰의 대표적인 방법으로 표본기록법과 일화기록법에 대해 학습하였습니다. 표본기록법과 일화기록법의 장단점을 비교한 후 공통점과 차이점을 서술하시오.
- 학교사회복지론] 한국 중·고등학생들이 가장 호소하는 문제상황을 파악하고, 학교사회복지실천을 통해서 이를 예방하거나 조기에 개입하는 방안을 제시하시오
- 장애인복지론] 장애인의 교육재활에 대한 내용을 정리하고 교육재활의 필요성과 교육재활에서의 지원방안을 개인의 견해를 담아 작성하시오
- 몬테소리의 교육관과 교육내용 및 방법 등을 현재 유아교육에 적용할 수 있는 부분과 유아교사에대한 시사점 토론을 통해 변화된 자신의 생각이나 교육관을 자유롭게 작성하시오
- 삼국시대 각각의 미용문화 특징의 장단점에 대하여 서술하시오
- 지적장애아동의 학습 특성에 대해 서술하고, 그러한 학습특성을 고려하여 장애통합 교사로서 어떻게 장애아동을 지도할 것인지 본인의 지도방법에 대해 서술하시오
해당 정보 및 게시물의 저작권과 기타 법적 책임은 자료 등록자에게 있습니다. 위 정보 및 게시물 내용의 불법적 이용,무단 전재·배포는 금지되어 있습니다. 저작권침해, 명예훼손 등 분쟁요소 발견 시 고객센터에 신고해 주시기 바랍니다.





















 분야
분야

